ハロゲン化アリールの結合解離エネルギー
はじめに
パラジウムやニッケルを使ったクロスカップリング反応では,ハロゲン化物の炭素-ハロゲン結合解離エネルギーによって反応性が変化することが知られています.これは,金属が炭素-ハロゲン結合に酸化的付加するために必要なエネルギーが,その結合解離エネルギーに依存する傾向にあるためです.このため,カップリング反応ハロゲン化アリール(ベンゼン,ピリジン,チオフェン)の炭素-ハロゲン結合解離エネルギーを目安に反応性を予測することができます.そこで,ハロゲン化アリール類の結合解離エネルギーをDFT計算によって求め,テーブルにまとめました.
なお,今回の計算で求めた結合解離エネルギーは,0 Kおける式(1)の反応のエネルギー変化です.
Ar–X → Ar• + X• (1)
計算結果
ZORA-(U)B3P86/TZVPレベルの計算により求めた炭素-ハロゲン結合解離エネルギーを表1にまとめます.なお,ピリジン,チオフェンの置換位置は図1のようになります.
表1.炭素-ハロゲン結合解離エネルギーD0 (ΔE+ZPE, ZORA-(U)B3P86/TZVP)
| ハロゲン化アリール |
結合解離エネルギー [kcal/mol] |
| ヨードベンゼン |
67.4 |
| ブロモベンゼン |
79.9 |
| クロロベンゼン |
91.3 |
| 2-ヨードピリジン |
62.8 |
| 3-ヨードピリジン |
67.5 |
| 4-ヨードピリジン |
66.2 |
| 2-ブロモピリジン |
75.7 |
| 3-ブロモピリジン |
79.5 |
| 4-ブロモピリジン |
78.7 |
| 2-クロロピリジン |
87.5 |
| 3-クロロピリジン |
90.8 |
| 4-クロロピリジン |
90.1 |
| 2-ヨードチオフェン |
71.1 |
| 3-ヨードチオフェン |
69.7 |
| 2-ブロモチオフェン |
82.2 |
| 3-ブロモチオフェン |
81.3 |
| 2-クロロチオフェン |
93.0 |
| 3-クロロチオフェン |
92.2 |
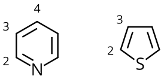
- 図1.ピリジン,チオフェンの置換位置
よく知られているように,炭素-ハロゲン結合解離エネルギーはCl > Br > Iの順番に小さくなります.また,ピリジンでは3位 > 4位 > 2位の順に結合解離エネルギーが小さくなります.チオフェンの場合は3位の方が2位よりも結合解離エネルギーが小さくなっており,ピリジンと逆の傾向にあります.
計算方法
DFT法でエネルギー計算または構造最適化および基準振動解析を行いました.汎関数にはB3P86を用い,基底関数には非縮約のTZVPを用いました.また,相対論効果をZORA/RI法で考慮しました.なお,ラジカルの計算は非制限法で行いました.結合解離エネルギーにはスケーリングなしの零点振動エネルギーを含んでいます.すべての計算はORCA
2.8.0で行いました.
なお汎関数の選択は,J. Phys. Chem. A2003, 107, 9991–9996を参考にしました.
